液体环境纳米红外光谱和成像系统
仪器简介
纳米红外光谱技术是一项从2013年起逐步受到学界广泛关注的技术。由于水溶液对红外光的强烈吸收,以及溶液环境的阻尼会显著干扰原子力显微镜探针运动,早期阶段的纳米红外光谱技术只能在大气环境中使用,难以表征液体环境中的研究对象,如电化学界面过程。
本团队在国家重大仪器研发项目的支持下,从零开始,经5年自主研发建起一个先进的液体纳米红外光谱技术研究平台,从物理原理、测控技术、环境控制、样品制备等多个基础角度开展了纳米红外光谱技术研究,分阶段逐步破解难题,先后搭建三代纳米红外光谱仪器。
第一代系统聚焦于建立技术基础,突破了软件、硬件、数据采集与算法等纳米红外光谱技术基础。第二代系统聚焦于突破限制瓶颈,发展底部激发模块,破解了纳米红外光谱技术受液体环境干扰的限制。第三代系统关注创新发展引领,设计电化学光谱环境池,率先实现对电化学界面过程的原位纳米红外光谱探测。最新的第三代仪器,首次实现电化学界面的纳米红外光谱和成像测量,以及与形貌、力学和电学的多模式关联成像,空间分辨率小于4 nm,检测灵敏度可达到对1.2 nm厚度分子膜的测量,处于国际领先水平。
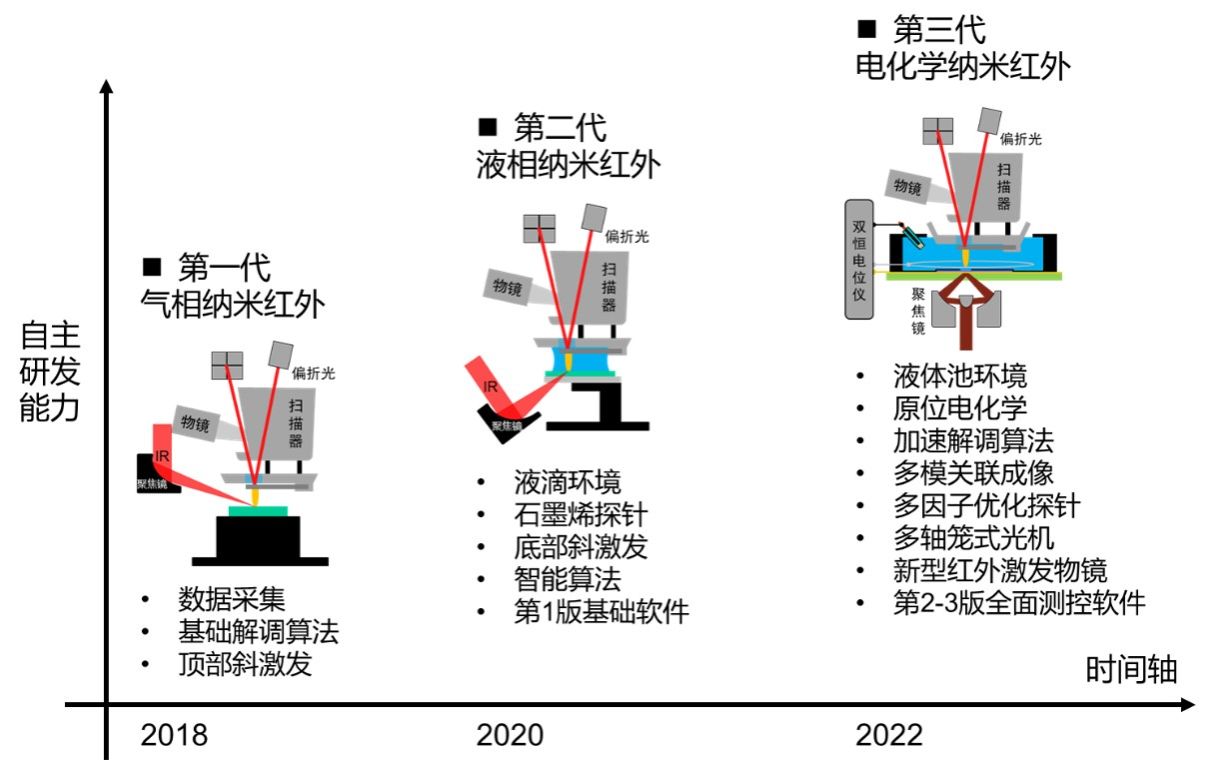
图1. 先后自主研发的3代液体环境纳米红外光谱仪器示意图,以及相对应的阶段性自主技术突破。
第三代电化学纳米红外光谱仪中,采用了订制的光谱电化学池。光谱电化学池的结构包括BaF2衬底、10 nm金膜工作电极。为适配光谱电化学池,采用数值孔径为0.5的反射式物镜从底部直接照射。光谱电化学池锁定在一个中空的三轴纳米位移平台表面,使系统突破探针扫描的局限,实现样品扫描。总体光机械结构采用多轴笼式系统,增加系统稳定性,同时兼顾开放性的特征。
在软件方面,团队自主开发了配套测控软件,可融合激光器控制、红外光脉冲触发等硬件功能,实现了纳米红外光谱和成像的精确测量。并将纳米红外光谱的解调算法模块化,通过触发频率-解调频率和红外振幅强度成像,显著提高红外光脉冲优化效率。此外还可实时输出红外信号到原子力显微镜控制器,实现关联形貌的纳米红外光谱成像。并特别增加了电化学控制模块,实现了电化学纳米红外光谱和成像测量。增加了样品扫描纳米位移平台,可搭配智能算法实现高速的纳米尺度红外高光谱成像。
经过系列研发,基于第三代电化学纳米红外光谱仪,团队实现了电化学界面的原位纳米红外光谱和成像测试,成功将纳米红外光谱技术推进到原位表征电化学界面的水准,是国际上首次实现电化学界面的原位纳米红外测量。

图2.(a)最新的第三代仪器设计的设计示意图。(b)装载在系统中的光谱电化学池照片。(c)光谱电化学池结构设计图。(d)第三代仪器装置实物照片,包括多轴笼式结构,光谱电化学池。
性能测试
采用滴涂、悬涂等技术制备了聚甲基丙烯酸甲酯(polymethyl methacrylate,PMMA)、聚碳酸酯(Polycarbonate,PC)、聚苯乙烯(polystyrene,PS)和PMMA的嵌段共聚物以及PS膜等标准样品。这些标准样品可以很好地表征仪器性能。
水环境和空气环境中,原子力显微镜探针在PMMA膜表面显示出明显差异的力曲线。在空气中探针自由震荡的振幅小,水溶液中自由震荡很快被水溶液衰减。在探针和样品膜刚好接触的时刻,空气中会出现“jump to contact”特征点,而在溶液中这一特征变得不明显。空气和水溶液中,同一样品膜表面获得的纳米红外光谱,信噪比基本一致,但溶液中的光谱会有更高的基线。固定激发波长为1730 cm-1,扫描样品表面的碳氧双键分布。形貌和化学成像互相位置关联。纳米尺度下碳氧双键表现出明显的异质分布。这一结果证实了液体环境纳米红外光谱仪器在水溶液中可稳定高性能地工作。
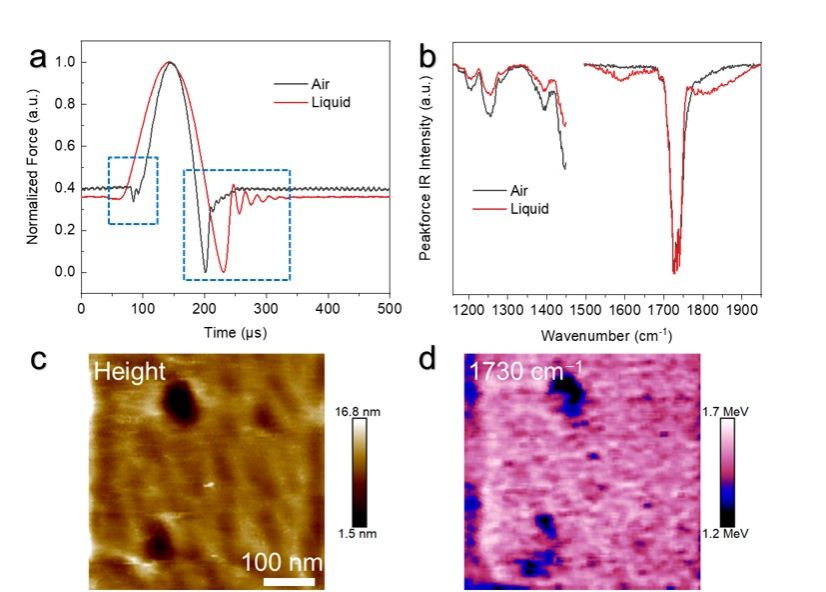
图3. 水环境标准样品聚合物膜表面的纳米红外测试。(a)水溶液和空气中,聚合物膜表面针尖的力曲线。方框表示出二者明显的不同。(b)空气和水溶液中PMMA膜的纳米红外光谱比较。(c)PMMA膜表面形貌图。(d)PMMA薄膜表面碳氧双键成像。
为表征仪器的检测灵敏度,研发团队采用LB(Langmuir-Blodgett,LB)膜技术在超薄金膜衬底表面制备了少层超薄样品。AFM形貌成像和1630 cm-1的纳米红外成像紧密关联。观察靠近衬底区域的薄层样品区,比较轮廓和纳米红外强度,结果表明在1.2 nm厚度的LB膜边缘,仪器的空间分辨率可达3.16 nm,优于国际报道的6 nm空间分辨率。进一步地,在衬底表面制备DNA双螺旋链,分别采用1280 cm-1和1700 cm-1成像。在DNA链的边缘可观察到类似螺旋结构的成像。这一实验结果表明,研发团队设计的液体环境纳米红外光谱仪的检测灵敏度可达到对1.2 nm厚度样品敏感的超灵敏程度,其空间分辨率好于国际报道中的最佳水平。
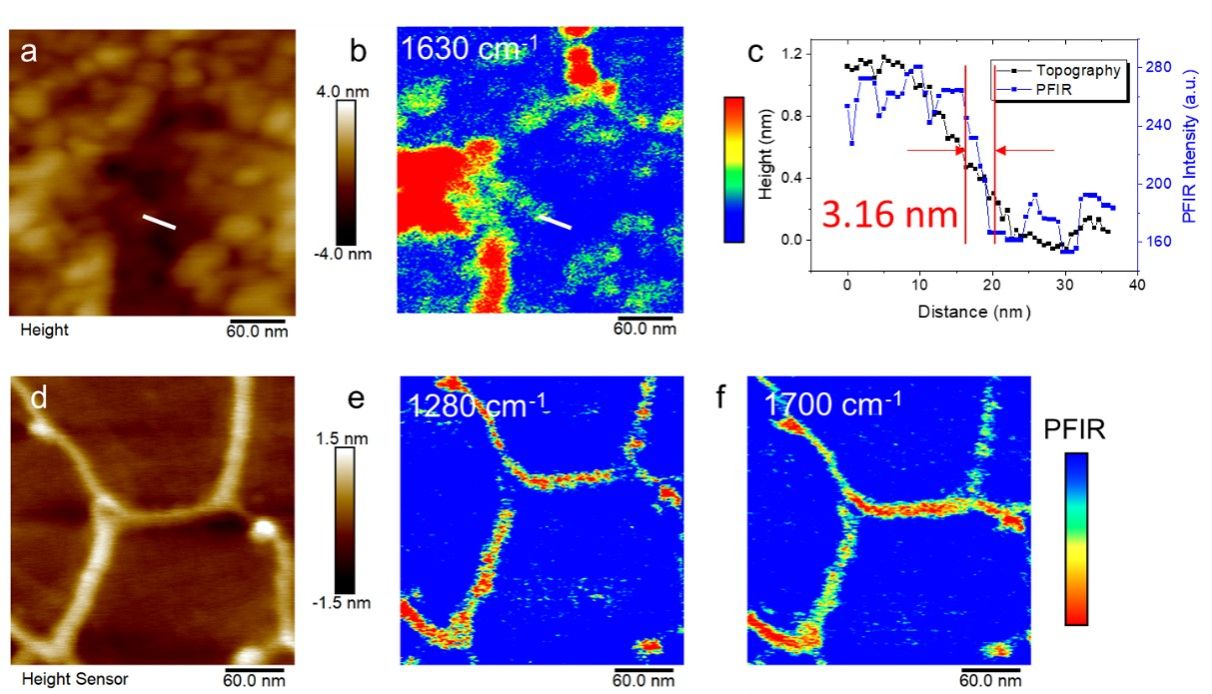
图4. 超薄样品膜的超灵敏超高空间分辨纳米红外成像测量。(a)LB膜技术制备的超薄样品AFM形貌成像。(b)1630 cm-1激发的关联纳米红外成像。(c)对形貌和纳米红外成像中的白色线条区域获得轮廓,比较纳米红外强度和相貌之间的关联性。(d)DNA链的形貌成像。(e)1280 cm-1激发时的纳米红外成像。(f)1700 cm-1激发时的纳米红外成像。
电化学过程的原位纳米红外光谱观察
选择苯胺电聚合这一经典电化学反应用于验证电化学纳米红外光谱技术对电极界面过程的原位监测能力。实验中红外光束从底部透过BaF2照射在探针-样品区域。电化学池中加入0.1 M硫酸和30 mM苯胺作为电解液进行循环伏安测试。电化学反应后,电极界面反应区域会表现出明显的颜色变化。聚合前主要是10 nm金膜的浅黄色,聚合后则是聚苯胺膜的墨绿色。循环伏安曲线记录了整个聚合反应过程,在0.21 v和0.1 v分别观察到苯胺电聚合过程的第一次氧化还原峰。该峰位随反应过程逐渐发生移动和增强。电流的增强除了与苯胺膜的聚合有关外,也与伴随聚合过程的电化学质子掺杂有直接联系。反应后的薄膜表面测量纳米红外光谱,可在谱图中观察到明显的3个谱峰,分别对应薄膜中的苯环结构和醌式结构。将激光器波长固定在1500 cm-1,跟踪整个反应过程中电极界面的变化过程,形貌成像可观察到不太显著的表面结构变化,但在化学成像通道,随反应进行,金电极表面的苯环骨架振动信号逐渐变强并显示出与形貌图案关联的异质分布特性。
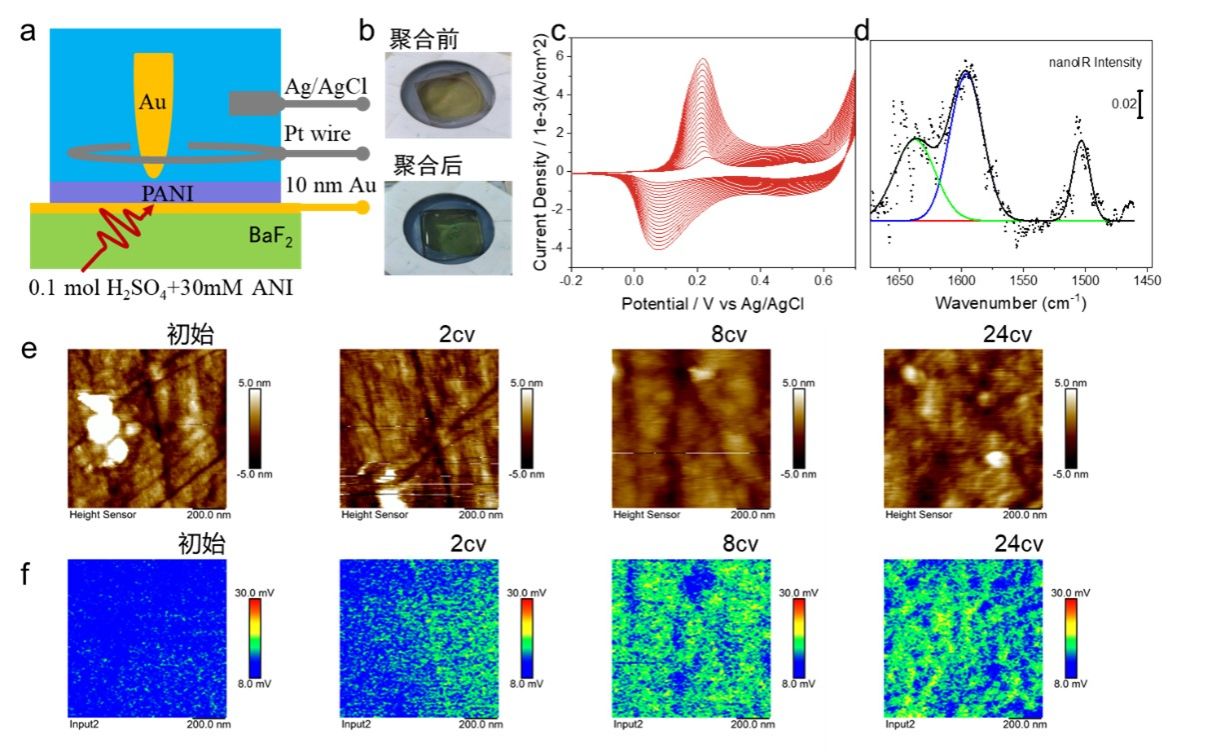
图5. 苯胺电聚合过程的原位纳米红外光谱观察。(a)实验装置结构示意图。(b)聚合前后电化学池电极反应区域颜色对比。(c)苯胺电聚合过程在-0.2 v-0.7 v间的40次循环伏安曲线。(d)电极表面聚苯胺膜的纳米红外光谱图,其中散点图为实测数据,黑色曲线为拟合光谱。(e)电化学过程中电极界面的形貌演变。(f)与形貌演变关联的纳米红外成像,激发波长为1500 cm-1。
